La diagnosi genetica preimpianto (DGP) è un'analisi genetica di embrioni ottenuti da fecondazione in vitro (FIV) con lo scopo di selezionare embrioni sani con capacità di impianto.
Inoltre, la DGP è la tecnica più indicata per evitare la trasmissione di una malattia genetica ereditaria, poiché permette di individuare gli embrioni con mutazioni nel loro DNA, che saranno scartati per il loro trasferimento nell'utero.
La DGP deve essere eseguita da esperti sia in embriologia che in genetica, in quanto richiede tecniche molto delicate come la biopsia blastometrica e le tecniche di genetica molecolare.
Di seguito trovate un indice con i 9 punti che tratteremo in questo articolo.
- 1.
- 2.
- 2.1.
- 2.2.
- 3.
- 3.1.
- 3.2.
- 4.
- 4.1.
- 4.2.
- 5.
- 6.
- 6.1.
- 6.2.
- 6.3.
- 6.4.
- 6.5.
- 7.
- 8.
- 9.
DGP passo dopo passo
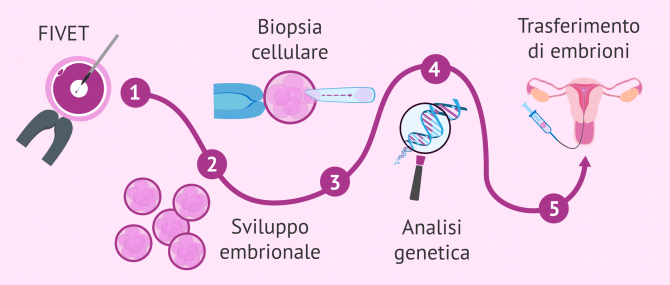
La FIV con DGP è uno dei trattamenti più laboriosi nella riproduzione assistita e quindi ha diversi passaggi dalla stimolazione ovarica al trasferimento embrionale. Li commentiamo qui di seguito:
- FIVET
- consiste nell'eseguire la stimolazione ovarica sulla donna, ottenere gli ovuli mediante puntura follicolare e, infine, fecondare gli ovuli con lo sperma del partner maschile o di una donatrice anonima.
- Sviluppo embrionale
- le caratteristiche degli embrioni in coltura sono valutate quotidianamente, poiché per poter eseguire la biopsia è necessario che abbiano un livello minimo di qualità per garantire la loro sopravvivenza.
- Biopsia cellulare
- estrazione di uno o più blastomeri (cellule dell'embrione) per la successiva analisi genetica. Può essere eseguita il giorno 3 embrioni o una volta che hanno raggiunto lo stadio di blastocisti il giorno 5. La cella rimossa viene poi accuratamente posizionata in un tubo, un processo noto come tubing.
- Analisi genetica
- studio dei cromosomi e / o geni nelle cellule biopsiate per identificare possibili alterazioni in essi. In particolare, l'analisi dei cromosomi è meglio conosciuta come screening genetico preimpianto e, d'altra parte, il termine DGP è usato per l'analisi di specifiche mutazioni genetiche.
- Trasferimento di embrioni
- gli embrioni geneticamente sani sono selezionati per il trasferimento nell'utero della madre o per la crioconservazione per tentativi futuri.
Va notato che il trasferimento di embrioni può essere effettuato in ciclo fresco o differito. Questo dipenderà dal tempo necessario per ottenere i risultati dell'analisi genetica, ed è abbastanza comune che gli embrioni debbano essere congelati.
Biopsia embrionale
La biopsia embrionale è il processo di estrazione di una o più cellule, chiamate blastomeri, per analizzare il DNA degli embrioni alla ricerca di eventuali alterazioni genetiche.
La vitalità dell'embrione può essere compromessa da questa biopsia, poiché la perdita di una cellula può essere troppo stressante per la sopravvivenza dell'embrione. Pertanto, è necessario che questa estrazione delle cellule sia effettuata da personale di laboratorio altamente specializzato ed esperto.
L'embriologo specialista in DGP, il dottor Antonio Alcaide, spiega le particolarità di questo processo:
La rimozione della cellula per l'analisi in una diagnosi preimpianto è fatta facendo una biopsia. Si deve praticare un piccolo foro nello strato più esterno dell'embrione e si deve rimuovere una delle cellule e poi si deve analizzare il DNA nel nucleo di quella cellula.
La biopsia embrionale può essere fatta il giorno 3 o il giorno 5. In entrambi i casi, è essenziale che la fecondazione avvenga attraverso un ICSI.
Nella FIV convenzionale, ci sono spermatozoi e cellule di granulosa attaccati alla zona pellucida dell'embrione. Ciò comporta un rischio di contaminazione dei blastomeri estratti e quindi la DGP potrebbe dare un risultato alterato.
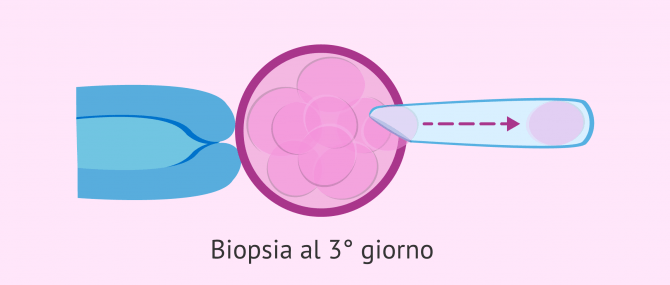
Biopsia del blastometro al 3° giorno
Al terzo giorno di sviluppo embrionale, gli embrioni di buona qualità hanno di solito 8 cellule, anche se possono avere tra le 6 e le 10 cellule a seconda del loro tasso di divisione.
Pertanto, se la biopsia viene fatta in questo preciso momento, solo uno, o al massimo due blastomeri saranno rimossi dall'embrione per non comprometterne la vitalità.
Durante la procedura, viene praticato un foro nella zona pellucida dell'embrione per mezzo di impulsi laser o agenti chimici, come l'acido Tyrodes. Una volta fatto questo foro, il blastometro viene rimosso per aspirazione.
Dopo la biopsia embrionale, ci sono due possibili opzioni per gli embrioni:
- Coltivo della blastocisti
- gli embrioni vengono lasciati in coltura per continuare la loro evoluzione in attesa dei risultati dell'analisi genetica. Pertanto, il trasferimento dell'embrione sarà in fase di blastocisti il giorno 5.
- Vitrificazione degli embrioni
- gli embrioni vengono congelati dopo la biopsia per il trasferimento in un ciclo successivo.
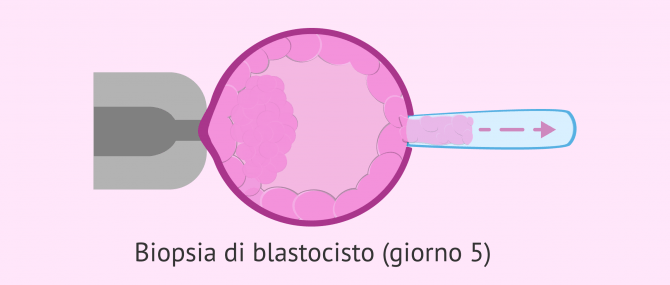
Biopsia del trofectoderma al 5° giorno
Al quinto giorno di sviluppo, l'embrione è diventato una cosiddetta blastocisti. Si tratta di un embrione più grande, composto da una moltitudine di cellule e con 3 parti differenziate:
- Massa della cellula interna (MCI)
- dà origine al futuro feto.
- Blastocele
- è una cavità interna riempita di fluido.
- Trophoectoderm
- strato esterno che dà origine alla placenta e ad altre strutture extra-embrionali.
Sebbene si tratti di popolazioni cellulari diverse, sia le cellule ICM che quelle trofoectodermiche hanno lo stesso materiale genetico. È quindi possibile estrarre alcune cellule da questo strato esterno per l'analisi con la DGP.
Il fatto che dall'embrione si possano estrarre più cellule è un vantaggio, poiché si otterrà un risultato più affidabile, sarà possibile individuare casi di mosaicismo e, inoltre, la vitalità dell'embrione non sarà così compromessa.
Quando si esegue la biopsia con una blastocisti, occorre fare attenzione a fare il foro in un luogo lontano dall'ICM per evitare possibili danni.
D'altra parte, è più conveniente utilizzare i brevi impulsi del laser per perforare la zona pellucida rispetto all'acido Tyrodes, poiché ha notevolmente ridotto il suo spessore man mano che la blastocisti si espande e l'uso di un agente chimico potrebbe danneggiarla.
Poi, una volta che è stato fatto un foro sufficiente per inserire la pipetta per biopsia, le cellule vengono rimosse per aspirazione. Per separare le cellule da rimuovere da quelle che rimangono all'interno dell'embrione, gli impulsi laser possono aiutare.
In questo caso, sarà necessario vitrificare gli embrioni dopo la biopsia per poterli trasferire in un ciclo futuro, poiché i risultati dell'analisi genetica richiedono diversi giorni e non sarebbe possibile lasciare gli embrioni in coltura.
Screening genetico pre-impianto
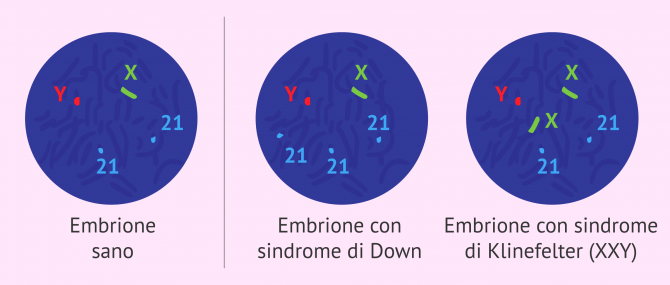
Lo screening genetico preimpianto, noto anche come PGS, è un tipo di DGP in cui vengono analizzate le possibili aneuploidie negli embrioni.
Le aneuploidie sono alterazioni del numero o della struttura dei cromosomi, tenendo conto che la normale dotazione di cromosomi umani è di 46 cromosomi. Pertanto, il guadagno o la perdita di un cromosoma, così come i cambiamenti nella sua struttura, sono anomalie che possono portare a embrioni non vitali o neonati con malattie cromosomiche come la sindrome di Down.
In alcune cliniche, questo tipo di DGP è anche chiamato screening di aneuploidiae i test genetici utilizzati per la loro individuazione sono quelli discussi nelle sezioni seguenti.
Studio FISH
L'ibridazione fluorescente in situ (FISH) è la tecnica tradizionalmente utilizzata nello studio delle anomalie cromosomiche.
Permette l'analisi solo di alcune regioni di 9 cromosomi (13, 15, 16, 17, 17, 18, 21, 22, X e Y). Tuttavia, questi cromosomi sono coinvolti in aneuploidie che possono portare a ripetuti aborti spontanei o alla nascita di bambini malati.
Il processo consiste nell'aggiunta di sonde fluorescenti per specifiche regioni dei cromosomi da analizzare. È quindi possibile visualizzare il segnale fluorescente attraverso uno speciale microscopio e rilevare se una delle regioni analizzate è mancante o, al contrario, se ci sono più copie di quante dovrebbero essere.
Poiché l'analisi solo di un certo numero di cromosomi è un limite, la FISH è considerata un'analisi incompleta ed è attualmente in fase di sostituzione con altre tecniche che permettono un'analisi genetica completa dell'embrione.
Array CGH
L'Array of Comparative Genomic Hybridization (A-CGH) è una tecnica che ci permette di effettuare uno screening dei cromosomi completo (CCS per nome in inglese Comprehensive Chromosome Screening ), cioè le 23 coppie di cromosomi vengono analizzate contemporaneamente alla ricerca di regioni con qualche alterazione cromosomica.
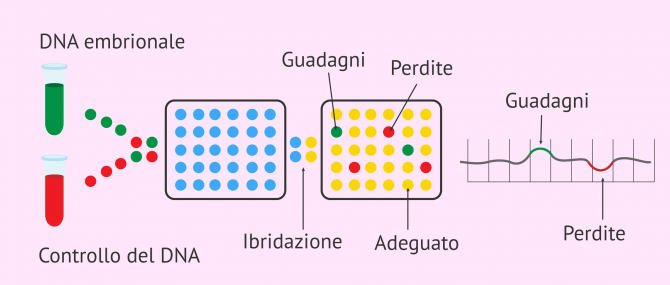
Per effettuare questa analisi genetica, si utilizza un DNA di controllo e il campione di DNA da studiare dalla cellula embrionale estratta. Entrambi i filamenti di DNA sono marcati con diverse sonde fluorescenti e poi ibridati nel microarray.
Con questa metodologia è possibile confrontare il DNA dell'embrione con quello del campione di riferimento e identificare perdite (delezioni) o guadagni (duplicazioni) di materiale genetico, che potrebbero portare a difetti embrionali.
Anche se questa tecnica è molto più determinante del FISH, fa solo confronti quantitativi, cioè rileva se c'è materiale genetico mancante o in eccesso. Pertanto, non rileva se ci sono frammenti cromosomici che non sono al posto giusto, come le inversioni o le traslocazioni.
DGP per le malattie monogeniche
Le malattie monogeniche sono quelle causate da mutazioni di un singolo gene, come la fibrosi cistica, l'emofilia o la fragile sindrome X.
Inoltre, sono malattie ereditarie che si trasmettono dai genitori ai figli. Pertanto, prima di fare la DGP sugli embrioni, è necessario identificare la mutazione specifica nei genitori attraverso uno studio di informatività.
Una volta localizzata la mutazione e determinato il tipo di ereditarietà (dominante, recessiva o legata al sesso), è possibile studiare gli embrioni con gli strumenti genetici descritti di seguito.
PCR
La reazione a catena della polimerasi (PCR) comporta l'amplificazione di specifiche sequenze di DNA per ulteriori analisi. In questo modo, è possibile ottenere milioni di copie del gene di interesse da una singola copia presente nella cellula estratta.
Una volta amplificata la sequenza desiderata, vengono utilizzate diverse tecniche di biologia molecolare per analizzarla e individuare le possibili mutazioni che danno origine a malattie monogeniche.
Sequenziamento masivo
Il sequenziamento di prossima generazione o NGS (del nome inglese Next-Generation Sequencing) è la tecnica più avanzata per gli studi genetici oggi.
I vantaggi che offre rispetto ad altre tecniche sono i seguenti:
- Permette lo studio di tutte le 23 coppie di cromosomi nella stessa analisi e con una risoluzione più alta.
- Permette l'analisi simultanea di oltre 500 geni associati a malattie ereditarie.
- È possibile studiare le aneuploidie e le malattie monogeniche separatamente o contemporaneamente in un'unica analisi.
- Riduzione dei tempi di analisi, evitando di congelare gli embrioni in attesa dei risultati.
- Consente di analizzare un numero elevato di campioni contemporaneamente, rendendo il costo dell'analisi più accessibile.
Al giorno d'oggi, sempre più cliniche stanno optando per questa tecnologia di ultima generazione sia per lo screening dell'aneuploidia che per l'individuazione di malattie monogeniche.
Trasferimento di embrioni sani
Una volta ottenuti i risultati, gli embrioni sani saranno trasferiti nell'utero della madre o vitrificati per futuri tentativi. Gli embrioni con alterazioni genetiche vengono scartati, anche se apparentemente hanno una buona qualità morfologica.
Se gli embrioni sono stati vitrificati prima dei risultati, saranno trasferiti in un ciclo sostitutivo. Per fare questo, la donna dovrà effettuare un preparato endometriale con la somministrazione di estrogeni e progesterone.
Se i risultati mostrano che ci sono diversi embrioni privi di anomalie, solo l'embrione o gli embrioni con la migliore qualità morfocinetica per il trasferimento saranno scongelati, il che aumenterà la probabilità di impianto.
Domande più frequenti
Qual è la probabilità che non ci siano più embrioni dopo la PGT?
Il Test Genetico Preimpianto (PGT) permette di individuare anomalie genetiche negli embrioni, prima del loro trasferimento nell'utero della donna. L'identificazione di embrioni privi di anomalie cromosomiche e mutazioni genetiche può impedire la loro trasmissione alla prole.
Più embrioni sono disponibili per la PGT, maggiori sono le possibilità di ottenere embrioni sani adatti al trasferimento nell'utero della donna. I progressi nella coltura embrionale e nelle tecniche di biopsia hanno permesso di effettuare l'analisi genetica degli embrioni allo stadio di blastocisti, permettendo di ottenere un numero maggiore di cellule (trofoectoderma) e di mantenere l'integrità dell'embrione e la sua capacità di impianto.
Tuttavia, la riserva ovarica e la risposta ovarica alla stimolazione della gonadotropina sono inversamente correlate all'età materna, poiché più la madre è anziana, più bassa è la riserva e la risposta. Di conseguenza, l'età materna avanzata influenza il numero di ovociti, la loro qualità e il numero di embrioni disponibili per la biopsia.
In quali casi viene utilizzata la DGP?
La DGP facilita il processo decisionale informato e viene sempre più inclusa come opzione nell'ambito di una corretta consulenza genetica.
L'obiettivo attuale è che può raggiungere qualsiasi coppia, se liberamente scelta, e qualsiasi patologia ereditaria, a condizione che vi sia un'indicazione clinica e che sia possibile affrontare tecnicamente la sua diagnosi.
Per quanto riguarda le coppie con una storia clinica di malattia monogenica, le principali indicazioni attuali sono, tra le altre, la fibrosi cistica, l'atrofia muscolare spinale, la distrofia miotonica (Steinert), la sindrome X fragile e la malattia di Huntington.
Per quanto riguarda l'analisi cromosomica, l'indicazione principale è lo studio embrionale dovuto al rischio di aneuploidia in età materna avanzata, senza dimenticare il gruppo di pazienti con una storia di aborto ricorrente e fattore maschile grave.
DGP e PGT sono la stessa cosa?
Questi sono gli acronimi per gli studi genetici che vengono eseguiti su un embrione prima che venga trasferito nell'utero. Da un lato, la DGP si riferisce alla diagnosi genetica preimpianto; mentre la PGT sta per Preimplantation Genetic Test.
Attualmente, il termine più comunemente usato per questa tecnica complementare è PGT.
Quali sono i vantaggi di fare una DGP?
Anche se un embrione ha un buon aspetto morfologico, può essere che geneticamente non sia normale e che porti al fallimento dell'impianto quando viene trasferito nell'utero o, peggio, ad una gravidanza non vitale che termina con un aborto spontaneo.
Può anche accadere che venga impiantato un embrione con qualche malattia cromosomica o alterazione genetica compatibile con la vita e, infine, che nasca un bambino con qualche malattia grave.
Grazie alla DGP, gli embrioni geneticamente sani possono essere selezionati prima di essere trasferiti nell'utero, riducendo i tassi di aborto e aumentando quelli dei neonati vivi.
La rimozione di una o più cellule dall'embrione può influire negativamente sul suo ulteriore sviluppo?
Sì, il processo può compromettere la vitalità dell'embrione, poiché la perdita di alcune cellule può essere troppo stressante per la sua sopravvivenza. Anche così, il tasso di sopravvivenza è molto alto, soprattutto quando la DGP viene fatta in blastocisti, poiché questi embrioni hanno un numero di cellule maggiore di quelli del terzo giorno e, quindi, sono in grado di recuperare più facilmente dopo la biopsia.
Comunità e Supporto
In inviTRA lavoriamo per rendere l'informazione mensile e rigorosa accessibile a tutti. Se questo articolo ti ha aiutato, considera di sostenerci affinché possiamo continuare ad accompagnare più persone nel loro cammino verso la genitorialità.
Bibliografia
Anthony Homer H. Preimplantation genetic testing for aneuploidy (PGT-A): The biology, the technology and the clinical outcomes. Aust N Z J Obstet Gynaecol. 2019 Apr;59(2):317-324. doi: 10.1111/ajo.12960. Epub 2019 Feb 27.
Rajesh Parikh F, Sitaram Athalye A, Jagannath Naik N, Jayaram Naik D, Ramesh Sanap R, Fali Madon P. Preimplantation Genetic Testing: Its Evolution, Where Are We Today?J Hum Reprod Sci . Oct-Dec 2018;11(4):306-314. doi: 10.4103/jhrs.JHRS_132_18.
Sciorio R, Anderson R. Fertility preservation and preimplantation genetic assessment for women with breast cancer.Cryobiology. 2020 Feb 1;92:1-8. doi: 10.1016/j.cryobiol.2019.12.001. Epub 2019 Dec 18.
Wilding M, Terribile M, Parisi I, Nargund G. Thaw, biopsy and refreeze strategy for PGT-A on previously cryopreserved embryos. Facts Views Vis Obgyn. 2019 Sep;11(3):223-227.
Domande più frequenti: 'Qual è la probabilità che non ci siano più embrioni dopo la PGT?', 'In quali casi viene utilizzata la DGP?', 'DGP e PGT sono la stessa cosa?', 'Quali sono i vantaggi di fare una DGP?' e 'La rimozione di una o più cellule dall'embrione può influire negativamente sul suo ulteriore sviluppo?'.
Autori e collaboratori

Tutto ciò che riguarda la riproduzione assistita sui nostri canali.