La sterilità maschile è l'incapacità dello sperma di un uomo di fecondare un ovulo. Pertanto, sarà difficile che si verifichi una gravidanza. Ci sono diversi fattori che possono portare all'infertilità maschile.
In particolare, l'infertilità maschile dovuta a una causa spermatica è la ragione più comune per gli uomini che hanno problemi di concepimento.
In questo caso, l'origine della sterilità si trova nelle alterazioni della qualità seminale, cioè degli spermatozoi. Queste alterazioni possono essere diagnosticate per mezzo di un seminogramma e alcune delle più frequenti sono l'astenospermia, la teratozoospermia e l’azoospermia.
Di seguito trovate un indice con i 12 punti che tratteremo in questo articolo.
- 1.
- 2.
- 2.1.
- 2.2.
- 2.3.
- 3.
- 4.
- 5.
- 6.
- 7.
- 7.1.
- 7.2.
- 8.
- 9.
- 10.
- 11.
- 12.
Cause
Durante la spermatogenesi (il processo di formazione degli spermatozoi), possono verificarsi una serie di fallimenti o errori che portano alla produzione di spermatozoi alterati, sia nella loro morfologia, concentrazione o mobilità.
Qualsiasi mancanza nella qualità del seme può rendere difficile o impossibile la fecondazione dell'ovulo, il che porterebbe a non ottenere una gravidanza in modo naturale. Pertanto, queste alterazioni nello sperma sono una causa di sterilità maschile.
Tuttavia, grazie alle tecniche di riproduzione assistita, gli uomini con problemi di fertilità possono diventare padri biologici. Con il progresso di questi trattamenti, il numero di spermatozoi necessari e la loro mobilità non sono più fattori determinanti per ottenere una gravidanza.
I parametri seminali utilizzati come riferimento per diagnosticare queste alterazioni sono quelli pubblicati dall'Organizzazione Mondiale della Sanità (OMS) nel 2010. Il test utilizzato per analizzarli è il seminogramma, chiamato anche spermogramma.
Quando non c'è alterazione dei parametri seminali, si parla di normozoospermia. In caso contrario, verrà diagnosticata una delle patologie menzionate nelle sezioni seguenti.
Alterazioni nella conta degli spermatozoi
Una delle cause dell'infertilità maschile dovuta al fattore spermatico è avere una quantità insufficiente di spermatozoi nell'eiaculato. Quando c'è un basso numero di spermatozoi, le possibilità che uno degli spermatozoi fecondi l'uovo e rimanga incinta sono ridotte.
A seconda della gravità dell'alterazione della concentrazione spermatica, si possono verificare diverse situazioni: oligozoospermia, criptozoospermia e azoospermia.
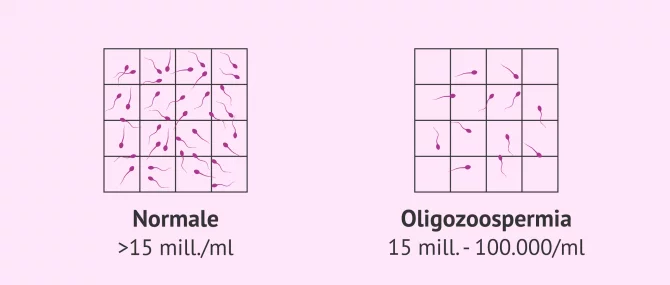
Oligozoospermia
L'oligozoospermia, chiamata anche oligospermia, è una bassa concentrazione di spermatozoi nel campione di sperma.
Secondo i valori di riferimento dell'OMS, un campione di sperma è normale quando ha almeno 15 milioni di spermatozoi per mL di eiaculato. Tuttavia, quando lo sperma contiene meno di questo valore ma più di 100.000 spermatozoi per mL di eiaculato, si dice che è un campione oligozoospermico.
Se vuoi continuare a leggere su questo argomento, puoi accedere a questo link: Cos'è l'oligospermia - Cause, tipi e trattamenti.
Criptozoospermia
La criptozoospermia si riferisce a una concentrazione troppo bassa di spermatozoi nel seme. In particolare, un uomo soffre di questa alterazione degli spermatozoi quando l'analisi del seme mostra un valore inferiore a 100.000 spermatozoi per mL di eiaculato. La criptozoospermia è quindi una variante dell'oligozoospermia.
Questa alterazione dello sperma può essere confusa con l'azoospermia o assenza di spermatozoi nell'eiaculato. In questi casi, se diagnosticato erroneamente come azoospermia, una biopsia testicolare sarà indicata inutilmente.
Se siete interessati a leggere di più su questo argomento, vi invitiamo a visitare il seguente articolo: Criptorchidismo: un disordine testicolare che causa infertilità.
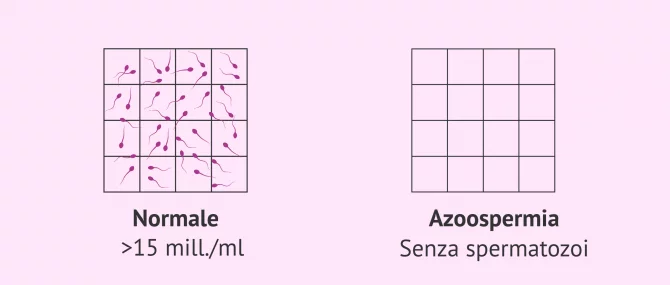
Azoospermia
L'azoospermia è definita come un problema seminale caratterizzato dall'assenza di spermatozoi nell'eiaculato. Questi uomini sono in grado di eiaculare, ma quando il campione viene analizzato, non si vedono spermatozoi.
A seconda della ragione di questa alterazione seminale, ci sono due tipi di azoospermia:
- Azoospermia ostruttiva
- causata da alterazioni nel trasporto dello sperma verso l'uretra.
- Azoospermia secretiva
- come risultato di problemi nella formazione dello sperma. Questo tipo di azoospermia è anche conosciuto come azoospermia non ostruttiva.
Va notato che se l'uomo ha avuto una vasectomia, l'azoospermia dovrebbe essere rilevata anche quando si analizza il campione di sperma. In caso contrario, significherebbe che la vasectomia non è stata efficace.
Per maggiori informazioni su questa alterazione seminale, vi consigliamo di leggere il seguente articolo: Cos'è l'azoospermia - Cause, diagnosi e trattamento.
Astenozoospermia
Il termine astenospermia è la parola usata per indicare quei casi in cui la mobilità degli spermatozoi è alterata. Secondo i parametri di riferimento dell'OMS, due tipi di motilità devono essere presi in considerazione nella valutazione della qualità dello sperma:
- Mobilità totale
- quanti spermatozoi si muovono.
- Mobilità progressivo
- quanti spermatozoi sono in grado di muoversi e spostarsi.
Così, per considerare un campione di sperma come normale, almeno il 40% degli spermatozoi deve essere motile e il 32% deve essere in grado di muoversi progressivamente. Altrimenti, il risultato seminale sarebbe l'astenospermia.
A seconda della gravità di questa alterazione, si distingue tra astenospermia grave, moderata o lieve.
Se vuoi saperne di più su questa alterazione seminale, puoi visitare il seguente articolo: Cos'è l'astenospermia - Definizione, cause e trattamento.
Teratozoospermia
La teratozoospermia è un'alterazione seminale che si riferisce alla forma degli spermatozoi. La morfologia normale di uno spermatozoo è:
- Testa ovale.
- Pezzo centrale o collo leggermente ispessito.
- Coda lunga e sottile.
Quando si studia un campione seminale di un maschio, almeno il 4% degli spermatozoi deve presentare queste caratteristiche per essere considerato un campione normale. Quando nell'eiaculato ci sono meno del 4% di spermatozoi con morfologia normale, questo campione di sperma sarà diagnosticato come teratozoospermia.
Ipospermia
Il concetto di ipospermia è definito come un volume di sperma inferiore a 1,5 ml dopo l'eiaculazione. Secondo i parametri di riferimento dell'OMS, il volume di un eiaculato normale dovrebbe essere compreso tra 1,5 e 6 ml.
Tra le cause di volumi di eiaculato anormali ci sono alterazioni delle vescicole seminali o dei dotti eiaculatori.
Anche se l'ipospermia può essere una causa di infertilità maschile, questo non è sempre il caso. La ragione principale è che se la concentrazione e la qualità dello sperma sono adeguate, il maschio sarà in grado di concepire senza problemi.
Se siete interessati a questo argomento, potete ottenere informazioni più complete nel seguente articolo: Ipospermia: scarsa eiaculazione di sperma negli uomini.
Necrospermia
Questo termine si riferisce ad un alto numero di spermatozoi morti. Per non essere considerata sterilità maschile per questa causa, è necessario che almeno il 58% degli spermatozoi presenti nell'eiaculato siano vivi.
Pertanto, se si trova un tasso di mortalità superiore al 58% nell'analisi del seme, verrà diagnosticata la necrospermia.
Combinazione di alterazioni seminali
In molte occasioni quello che succede è che un uomo soffre di diverse alterazioni seminali simultaneamente a causa di una cattiva produzione di sperma. Alcuni esempi sono mostrati qui sotto.
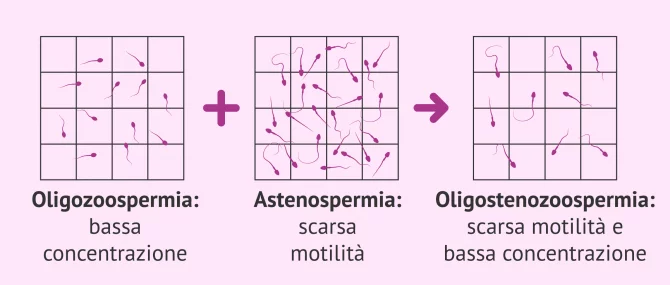
Oligoastenozoospermia
L'oligoastenozoospermia si verifica quando ci sono problemi di bassa concentrazione di spermatozoi e scarsa motilità dello sperma nello stesso maschio. Pertanto, l'oligoastenozoospermia è la combinazione di oligospermia e astenospermia.
Questi campioni seminali hanno una concentrazione di sperma inferiore a 15 milioni/ml e una motilità spermatica progressiva inferiore al 32%.
I maschi con oligoastenozoospermia avranno difficoltà a ottenere una gravidanza in modo naturale, poiché le possibilità che gli spermatozoi fecondino l'ovulo sono inferiori.
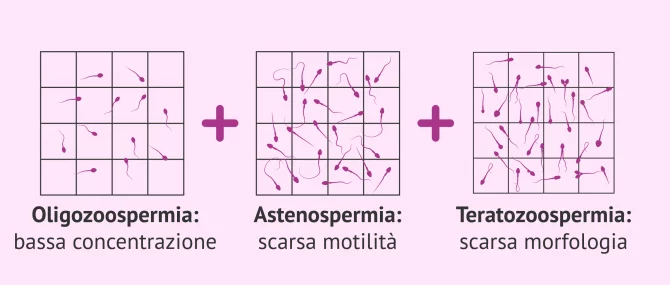
Oligoastenoteratozoospermia
Nei casi di oligoastenoteratozoospermia, c'è una combinazione delle seguenti alterazioni dello sperma:
- Bassa concentrazione di spermatozoi: meno di 15 milioni/ml di eiaculato.
- Scarsa motilità dello sperma: meno del 32% dello sperma si muove e si sposta.
- Scarsa morfologia dello sperma: meno del 4% degli spermatozoi ha una morfologia normale.
La possibilità di ottenere una gravidanza quando c'è questa alterazione seminale dipenderà dalla gravità dell'alterazione. Pertanto, è essenziale fare una buona diagnosi per stabilire il miglior trattamento.
Trattamento
La qualità dello sperma è uno dei fattori determinanti quando si indicano i trattamenti di riproduzione assistita. Quindi, a seconda di questo e in assenza di altre alterazioni che rendono difficile ottenere la gravidanza, sarà indicato:
- Inseminazione artificiale
- quando la qualità seminale è buona secondo i parametri sopra menzionati, ma la gravidanza non si ottiene naturalmente.
- Fecondazione in vitro (FIVET)
- nei casi in cui la qualità seminale è alterata. Quei pazienti che hanno gravi alterazioni, l'ICSI sarà la loro unica opzione.
- Biopsia testicolare
- sarà necessario se viene diagnosticata l'azoospermia, per esempio.
Tuttavia, bisogna considerare che ogni caso deve essere valutato individualmente, poiché ci sono altri fattori come la storia medica della coppia o la fertilità della donna che possono influenzare la scelta di un trattamento o di un altro.
Domande più frequenti
Comunità e Supporto
In inviTRA lavoriamo per rendere l'informazione mensile e rigorosa accessibile a tutti. Se questo articolo ti ha aiutato, considera di sostenerci affinché possiamo continuare ad accompagnare più persone nel loro cammino verso la genitorialità.
Bibliografia
Adamopoulos DA. Medical treatment of idiopathic oligozoospermia and male factor subfertility. Asian J Androl. 2000;2(1):25-32.
Aitken RJ, Buckingham DW, Brindle, J, Gomez E, Baker HWG, Irvine DS (1995): Analysis of sperm movement in relation to the oxidative stress created by leukocytes in washed sperm preparations and seminal plasma. Hum Reprod 10:2061–2070.
Auger J, Jouannet P, Eustache F. Another look at human sperm morphology. Hum Reprod. 2016;31(1):10-23.
Bollendorf A, Check JH, Lurie D. Evaluation of the effect of the absence of sperm with rapid and linear progressive motility on subsequent pregnancy rates following intrauterine insemination or in vitro fertilization. J Androl 1996; 17550-7.
Dahlberg B (1988): Sperm motility in fertile men and males in infertile units: In vitro test. Arch Androl 20:31-34.
Francavilla F, Romano R, Santucci R, Poccia G. Effect of sperm morphology and motile sperm count on outcome of intrauterine insemination in oligozoospermia and/or asthenozoospermia. Fertil Steril. 1990;53(5):892-7.
Shabtaie SA, Gerkowicz SA, Kohn TP, Ramasamy R. Role of Abnormal Sperm Morphology in Predicting Pregnancy Outcomes. Curr Urol Rep. 2016;17(9):67.
World Health Organization (WHO) (2010). WHO laboratory Manual for the examination of human semen and sperm-cervical mucus interaction. Cambridge Academic Press.
Autori e collaboratori