La diagnosi genetica preimpianto (DGP) è una tecnica di prevenzione utilizzata nella riproduzione assistita per individuare anomalie nel materiale genetico degli embrioni.
Grazie alla DGP è possibile evitare il trasferimento di embrioni con alterazioni genetiche o cromosomiche e quindi aumentare la probabilità di avere un figlio sano.
La DGP è spesso chiamata anche PGD (preimplantational genetic diagnosis) ed è considerata una tecnica complementare che può essere applicata nel corso della fecondazione in vitro (FIVET).
Di seguito trovate un indice con i 10 punti che tratteremo in questo articolo.
- 1.
- 2.
- 3.
- 4.
- 4.1.
- 4.2.
- 4.3.
- 4.4.
- 5.
- 6.
- 6.1.
- 6.2.
- 6.3.
- 6.4.
- 6.5.
- 6.6.
- 6.7.
- 6.8.
- 6.9.
- 6.10.
- 7.
- 8.
- 9.
- 10.
Cos'è la DGP?
Sebbene, in generale, il termine Diagnosi Genetica Preimpianto o DGP sia usato per indicare l'uso di questa tecnica, la verità è che si distinguono due concetti a seconda dello scopo:
- Diagnosi genetica preimpianto o PGD
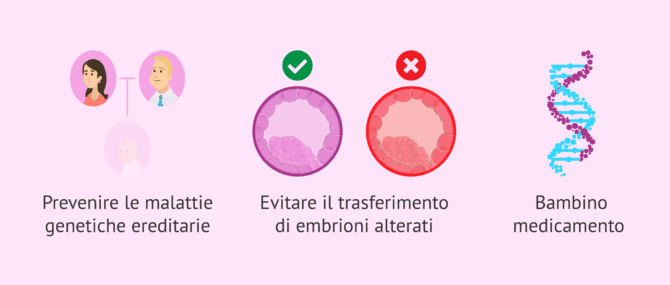
- permette la diagnosi precoce di gravi malattie genetiche, che possono essere trasmesse alla prole se i genitori sono portatori o malati. In generale, si tratta di malattie ereditarie monogeniche come la sindrome X-Fragile, la malattia di Huntingon e la distrofia muscolare.
- Screening genetico pre-impianto o PGS
- chiamato anche screening per aneuploidia. In questo caso si identificano alterazioni del numero o della struttura dei cromosomi. La malattia cromosomica più conosciuta è la sindrome di Down.
A seconda che si debbano rilevare alterazioni genetiche o cromosomiche, le tecniche di analisi del DNA degli embrioni saranno diverse.
Quando fare una DGP?
Gli specialisti della genetica e della fertilità consiglieranno di effettuare una PGD per avere un figlio nei seguenti casi:
- Quando i genitori, o almeno uno di loro, sono portatori di una malattia genetica ereditaria.
- Quando i genitori, o almeno uno di loro, hanno un cariotipo alterato (studio cromosomico). Ad esempio, possono essere portatori di traslocazioni o inversioni cromosomiche.
- Quando i genitori hanno già un figlio malato di una malattia che richiede un trapianto di cellule del sangue e decidono di avere un altro figlio sano e compatibile. E' quello che si chiama farmaco bambino.
- Dopo diversi fallimenti ripetuti nei cicli di FIVET.
- Dopo diversi fallimenti di impianto embrionale.
- Quando ci sono aborti ripetuti.
- Quando la donna è in età materna avanzata (consigliato per le donne sopra i 38-40 anni).
- Se c'è una storia di gravidanza aneuploide (numero sbagliato di cromosomi)
- In casi specifici di sterilità maschile, quando è necessario ottenere lo sperma dall'epididimo o dal testicolo, per esempio.
Procedura
Per poter eseguire la PGD sugli embrioni, la coppia o la donna deve essere sottoposta a un trattamento di FIVET. Pertanto, il primo passo è quello di eseguire una stimolazione ovarica che permette di ottenere un elevato numero di ovuli da fecondare.
Dopo la puntura ovarica, gli ovuli vengono fecondati con la tecnica ICSI (iniezione intracitoplasmatica di spermatozoi) per ottenere embrioni.
La DGP può essere fatta sia su embrioni di 3 giorni in coltura che su blastocisti di 5 giorni. In quest'ultimo caso, è possibile estrarre un numero maggiore di cellule dal trofoectoderma per effettuare lo studio genetico.
I passi per fare la DGP su ciascuno degli embrioni sono i seguenti:
- Biopsia embrionale: si pratica un foro nella zona pellucida dell'embrione utilizzando un laser o prodotti chimici per rimuovere una o due cellule, se l'embrione ha 3 giorni di vita, o diverse cellule dal trofoectoderma nel caso di blastocisti.
- Tubing: le cellule rimosse vengono delicatamente inserite in un tubo. Successivamente, il materiale genetico contenuto in ogni cellula sarà estratto.
- Analisi del DNA estratto: esistono diverse tecniche come FISH, CGH array, PCR o sequenziamento.
- Valutazione dei risultati: gli embrioni geneticamente sani e quelli con alterazioni del loro materiale genetico sono identificati e saranno scartati.
Infine, viene valutata la qualità degli embrioni che sono geneticamente vitali per il trasferimento nell'utero della madre. D'altra parte, gli embrioni rimanenti saranno vetrificati per i futuri tentativi.
Pro e contro
La DGP applicata alla prevenzione di gravi malattie ereditarie ha un chiaro vantaggio, in quanto evita alla coppia di dover decidere se interrompere la gravidanza per il trasporto di un bambino malato.
D'altra parte, la DGP per trattare l'infertilità e aumentare i tassi di successo fa nascere un dibattito tra sostenitori e detrattori della tecnica a causa delle considerazioni etiche in gioco.
Commenteremo ora i vantaggi e gli svantaggi della PGD, oltre ad alcuni aspetti etici e legali.
Vantaggi della DGP
Le persone che scelgono di fare la PGD durante la ricerca della gravidanza possono ottenere i seguenti benefici:
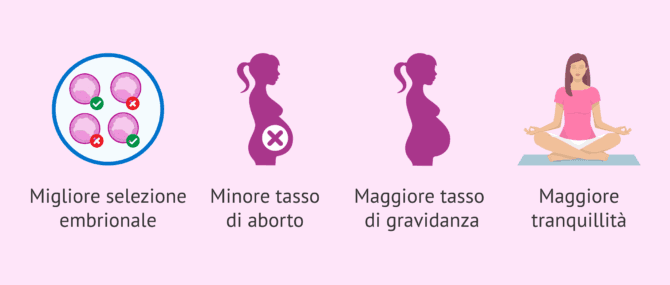
- La migliore selezione di embrioni
- ovviamente, l'obiettivo principale della PGD è quello di individuare gli embrioni geneticamente sani. Pertanto, è già possibile escludere direttamente quelle con mutazioni o aneuploidie che, senza questa analisi genetica, potrebbero essere confuse e trasferite alla madre, il che porterebbe al fallimento dell'impianto, all'aborto o alla nascita di un bambino malato.
- Riduzione del rischio di aborto
- alcune alterazioni cromosomiche permettono all'embrione di impiantarsi, ma dopo diverse settimane di sviluppo finiscono in un aborto spontaneo perché non hanno la corretta dotazione genetica.
- Tasso di gravidanza più alto
- in quanto gli embrioni che portano a ripetuti fallimenti di impianto sono evitati.
- Meno trattamenti FIVET
- la PGD permette di "fare bene" nella selezione dell'embrione con la maggiore capacità di impianto e che può dare origine a un bambino sano. Pertanto, il numero di trasferimenti non riusciti si riduce, così come il tempo per ottenere una gravidanza.
- Maggiore tranquillità per i pazienti
- la PGD riesce ad eliminare l'incertezza sul fatto che l'embrione sia buono o meno. Inoltre, una volta raggiunto il positivo, la donna si sente anche più rilassata sapendo che l'embrione è vitale e il rischio di aborto spontaneo è molto più basso.
Come abbiamo già detto, l'applicazione della tecnica della PGD riduce il numero di trattamenti di fecondazione in vitro. Inoltre, ciò comporta anche il vantaggio di diminuire il costo economico dell'investimento.
Svantaggi della DGP
L'applicazione della DGP ha anche, come le altre tecniche di riproduzione assistita, alcuni svantaggi:
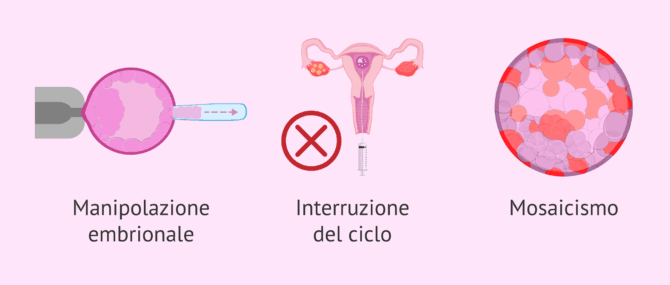
- Manipolazione di embrioni
- la biopsia embrionale è una procedura invasiva che consiste nel praticare un foro nella zona pellucida e, inoltre, nel passare più tempo al di fuori dell'incubatrice. Alcuni embrioni non possono resistere a questo processo e bloccare il loro sviluppo.
- Annullamento del ciclo
- Il DGP comporta la necessità di scartare diversi embrioni a causa del risultato anomalo. Se la coppia non ha avuto molti embrioni dopo la fecondazione, il rischio di dover annullare il trasferimento è maggiore.
- Mosaicismo
- alcuni embrioni hanno una miscela di cellule normali e cellule alterate. Pertanto, quando viene biopsiata una sola cellula dell'embrione, un embrione a mosaico non vitale può essere preso come sano, o viceversa.
Gli altri svantaggi della DGP hanno a che fare con gli aspetti etici e morali, di cui parleremo nella prossima sezione.
Polemiche etiche della DGP
Alcune persone, a causa del loro credo o della loro religione, considerano che la vita inizia nel momento stesso della fecondazione. Non sono quindi favorevoli a scartare gli embrioni che potrebbero portare ad una vita, così come non lo sono quelli che sono contro l'aborto.
D'altra parte, non considerano etico rifiutare embrioni che potrebbero portare a bambini con la sindrome di Down, la sindrome di Turner o altre malattie genetiche.
Queste sono alcune delle questioni etiche e morali che entrano nel dibattito sulla PGD e la sua attuazione:
- È etico selezionare embrioni sani e scartare quelli portatori di una malattia?
- È etico selezionare un embrione in modo che alla nascita possa aiutare a curare la malattia di un membro della famiglia?
- È etico scegliere il sesso dell'embrione o le sue caratteristiche fisiche?
- Le coppie che si sottopongono a tecniche di FIV hanno il diritto di conoscere il genoma dei loro embrioni?
- La DGP per le malattie a insorgenza tardiva è etica?
- Dov'è il limite nella selezione genetica degli embrioni?
Proprio a causa delle controversie che genera, questa tecnica riproduttiva non è legalizzata in molti paesi e, se la legge lo permette, alcune restrizioni sono di solito contemplate.
Aspetti legali della DGP
In contrasto con quanto succede in Italia, grazie alla pionieristica Legge 14/2006 sulle Tecniche di Riproduzione Umana Assistita, la diagnosi genetica preimpianto è una tecnica consentita in Spagna. Ecco perché è una destinazione adatta ai pazienti italiani Tuttavia, per la sua attuazione devono essere soddisfatti determinati requisiti:
- Nel caso di malattie genetiche ereditarie, queste devono essere considerate gravi, di insorgenza precoce e senza alcun trattamento curativo post-natale.
- Per le restanti alterazioni cromosomiche, la DGP può essere applicata per prevenire il trasferimento di embrioni con vitalità compromessa.
- Infine, la PGD può essere utilizzata come metodo terapeutico per curare un bambino malato (bambino medico), selezionando gli antigeni HLA della futura prole. Questa pratica richiede l'espressa autorizzazione della Commissione Nazionale per la Riproduzione Umana Assistita (CNRHA).
La legalizzazione della DGP in Spagna ha permesso al nostro paese di essere una delle principali destinazioni per la cosiddetta turismo riproduttivo. Va notato che l'uso della DGP è molto limitato in paesi come l'Italia o la Germania.
Prezzo
La diagnosi genetica pre-impianto è una complessità aggiunta al processo abituale di fecondazione in vitro, quindi il costo economico è più alto.
In generale, il costo della PGD può essere di circa 3.000-4.000 EUR in più rispetto alla procedura FIV-ICSI. Questo prezzo dipenderà dal fatto che si analizzino solo i cromosomi di base utilizzando FISH, quelli di base con alcuni o tutti i cromosomi.
Inoltre, il prezzo della PGD è influenzato anche da altri fattori come l'età della donna, la tecnica utilizzata per l'analisi, ecc.
I centri di riproduzione assistita di solito abbattono i prezzi in modo che i pazienti possano vedere quanto costa ogni parte del trattamento completo, oltre alla consueta biopsia embrionale e agli studi genetici.
Va notato che il prezzo finale di un ciclo FIVET con DGP dipende anche da ogni clinica della fertilità e da ogni singolo caso. Tuttavia, per avere un'idea dei prezzi, il budget è di solito tra gli 8.000 e i 9.000 euro
Domande più frequenti
Quanto tempo ci vuole per i risultati della DGP?
Il tempo in cui vengono forniti i risultati della DGP è di solito tra le 2 e le 4 settimane, anche se questi possono variare a seconda della tecnica, del laboratorio di genetica, ecc. Allo stesso modo, alcuni laboratori offrono la possibilità di effettuare una diagnosi in 24 ore, anche se questi casi sono solitamente studiati, sia per i costi che per i rischi associati.
Un aspetto importante è il caso in cui è necessario un precedente studio genetico per analizzare le malattie ereditarie. Questi casi implicano uno studio precedente variabile a seconda della patologia e della conoscenza della malattia che può raggiungere i 2 mesi. Dopo questo periodo di tempo, il trattamento di riproduzione assistita deve essere effettuato, che si concluderà con la diagnosi genetica. Vale a dire che questo processo può richiedere fino a 4 mesi.
Il test genetico preimpianto (PGT) può ridurre il rischio di aborto?
La Dott.ssa Marta Zermiani, ginecologa presso la clinica Vida Fertility Institute di Madrid, ci dà la risposta in questo video se il test genetico preimpianto (PGT) può ridurre il rischio di aborto:
Il test genetico preimpianto è una tecnica che si utilizza normalmente per cercare di capire se gli embrioni sono normali dal punto di vista genetico. Quindi, tendenzialmente, il risultato ci permette di trasferire solo gli embrioni sani e questo riduce il rischio di aborto.
Normalmente si raccomanda in persone che hanno più rischio di embrioni alterati e quindi più rischio di aborto. Quindi sì, basicamente è una tecnica che ci permette di ridurre gli aborti.
Quando è raccomandata la DGP?
In linea generale, l'esecuzione di un test genetico preimpianto (PGT, precedentemente chiamato DGP) sarebbe consigliata in situazioni quali:
- Rischio di trasmettere una malattia genetica al bambino, perché un genitore è affetto da una malattia genetica a eredità dominante o entrambi i genitori sono portatori di mutazioni per una malattia genetica recessiva.
- Cariotipo alterato in uno o entrambi i genitori.
- Aborto ricorrente.
- Precedenti fallimenti in cicli di FIV.
- Età della donna superiore a 38-40 anni, per il maggior rischio di aneuploidie.
- Fattore maschile severo, FISH degli spermatozoi alterato o quando si utilizzano spermatozoi ottenuti dal testicolo o dall'epididimo.
In ogni caso, l'equipe medica responsabile del trattamento di riproduzione assistita valuterà ogni singolo caso per vedere se l'esecuzione di un PGT sia indicata o meno.
Quanto è importante l'applicazione della PGD alle donne che decidono di diventare madri in età avanzata?
Dal punto di vista riproduttivo, se impostiamo come donne in età materna avanzata che cercano una gravidanza da 40-41 anni, i dati clinici sono chiari e rivelano che gli ovuli di queste donne hanno aumentato il rischio di alterazioni cromosomiche, soprattutto trisomie come il cromosoma 21 o la sindrome di Down.
I dati clinici dei principali gruppi medici che applicano la DGP mostrano che il suo utilizzo per questo gruppo di donne favorisce il tasso di gestazione e riduce il tasso di aborto.
La biopsia embrionale può causare anomalie nell'embrione?
La biopsia embrionale viene eseguita in una fase precoce dello sviluppo embrionale, quindi l'embrione è in grado di continuare a svilupparsi e di compensare la piccola quantità di cellule prelevate. È vero che l'embrione può subire danni durante la procedura e non sopravvivere, ma si tratta di un evento raro.
Posso effettuare il trasferimento di embrioni il terzo giorno se i miei embrioni sono PGD?
Attualmente, più del 90% delle biopsie embrionali per la PGD vengono eseguite il giorno 5, rendendo impossibile il trasferimento degli embrioni il giorno 3. Anche così, nei casi in cui la biopsia viene fatta il giorno 3, il risultato non sarà disponibile fino al giorno 5, quindi gli embrioni saranno trasferiti nello stadio di blastocisti il giorno 5.
Perché la DGP è adatta alle donne dai 40 anni in su?
Con l'avanzare dell'età della donna, la qualità degli ovuli diminuisce ed è più probabile che presentino alterazioni cromosomiche note come aneuploidie.
Pertanto, eseguire un PGT (test genetico preimpianto) sugli embrioni eviterebbe il trasferimento nell'utero di un embrione che presenta alterazioni cromosomiche che potrebbero portare ad un aborto spontaneo o alla nascita di un bambino con una malattia cromosomica come la sindrome di Down.
Quanti embrioni bisogna avere per fare una DGP?
In realtà non è necessario che ci sia un numero minimo specifico di embrioni per poter eseguire un test genetico preimpianto (PGT).
Tuttavia, in alcuni casi in cui il numero di embrioni da analizzare è ridotto, può essere consigliabile iniziare una nuova stimolazione ovarica per accumulare embrioni prima di eseguire il PGT, poiché si tratta di una tecnica economicamente costosa.
La DGP è a rischio?
Quando si esegue un PGT (precedentemente denominato DGP), l'embrione può essere danneggiato durante la biopsia embrionale, ma la possibilità che ciò accada è minima e la stragrande maggioranza degli embrioni sopravvive alla procedura.
D'altra parte, quando si ricevono i risultati del PGT, può accadere che nessuno degli embrioni analizzati abbia ottenuto un risultato favorevole. In questo caso, sarebbe necessario annullare il ciclo senza effettuare il trasferimento embrionale.
Esiste un'alternativa alla DGP per evitare alterazioni genetiche?
In alternativa al PGT (test genetico preimpianto) per evitare alterazioni genetiche nella prole, è possibile eseguire un test diagnostico genetico prenatale come l'amniocentesi o la biopsia dei villi coriali.
Tuttavia, è importante tenere presente che, trattandosi di test prenatali, vengono effettuati quando la gravidanza è già in corso. Se il risultato mostra che il bambino ha un'alterazione genetica e non si desidera portare avanti la gravidanza, sarebbe necessario ricorrere a un'interruzione volontaria di gravidanza (IVG).
Infine, un'altra possibile alternativa sarebbe quella di sostituire i gameti del genitore o dei genitori portatori dell'alterazione genetica con ovuli e/o spermatozoi di un donatore.
Lettura consigliata
Come abbiamo detto, la PGD è una tecnica complementare realizzata nel corso della fecondazione in vitro. Se volete sapere in cosa consiste questo trattamento, potete inserire il seguente post: Cos'è la FIVET?
Comunità e Supporto
In inviTRA lavoriamo per rendere l'informazione mensile e rigorosa accessibile a tutti. Se questo articolo ti ha aiutato, considera di sostenerci affinché possiamo continuare ad accompagnare più persone nel loro cammino verso la genitorialità.
Bibliografia
Bick, D.P. y Lau, E.C. (2006). Diagnóstico genético preimplantacional. Pediatr. Clin. N. Am., 53: 559 – 577.
Delhanty, J.D.A. and Handyside, A.H. (1995) The origin of genetic defects in the human and their detection in the preimplantation embryo. Hum. Reprod. Update, 1, 201–215 (Vedi)
Dokras, A., Sargent, I.L., Ross, C. et al. (1990) Trophectoderm biopsy in human blastocysts. Hum. Reprod., 5, 821–825 (Vedi)
Ermanno Greco, Katarzyna Litwicka, Maria Giulia Minas, Elisabetta Cursio , Pier Francesco Greco, Paolo Barillari. Preimplantation Genetic Testing: Where We Are Today. Int J Mol Sci
. 2020 Jun 19;21(12):4381. doi: 10.3390/ijms21124381 (Vedi)
Gleicher, N., Kushnir, V.A. & Barad, D.H. (2014). Preimplantation genetic screening (PGS) still in search of a clinical application: a systematic review. Reproductive Biology and Endocrinology, 12:22 (Vedi)
Ilana Löwy. ART with PGD: Risky heredity and stratified reproduction. Reprod Biomed Soc Online. 2020 Nov 5;11:48-55. doi: 10.1016/j.rbms.2020.09.007 (Vedi)
Manuel Viotti. Preimplantation Genetic Testing for Chromosomal Abnormalities: Aneuploidy, Mosaicism, and Structural Rearrangements. Genes (Basel). 2020 May 29;11(6):602. doi: 10.3390/genes11060602 (Vedi)
Martine De Rycke, Veerle Berckmoes. Preimplantation Genetic Testing for Monogenic Disorders. Genes (Basel). 2020 Jul 31;11(8):871. doi: 10.3390/genes11080871 (Vedi)
Moreno, J.M. (2007). Biopsia embrionaria. Aspectos técnicos. ASEBIR, 12: 17-21 (Vedi)
Rodrigo, L.; Rubio, C.; Mateu, E. y Buendía, P., 2014. Capítulo 14: El laboratorio de diagnóstico genético preimplantacional. Instituto Universitario IVI Valencia. Máster en Biotecnología de la Reproducción Humana Asistida. 9ª Edición (2014-2016). 1213-1277
Domande più frequenti: 'Quanto tempo ci vuole per i risultati della DGP?', 'Il test genetico preimpianto (PGT) può ridurre il rischio di aborto?', 'Quando è raccomandata la DGP?', 'Quanto è importante l'applicazione della PGD alle donne che decidono di diventare madri in età avanzata?', 'La biopsia embrionale può causare anomalie nell'embrione?', 'Posso effettuare il trasferimento di embrioni il terzo giorno se i miei embrioni sono PGD?', 'Perché la DGP è adatta alle donne dai 40 anni in su?', 'La DGP vi permette di scegliere il sesso del bambino?', 'Quanti embrioni bisogna avere per fare una DGP?', 'La DGP è a rischio?' e 'Esiste un'alternativa alla DGP per evitare alterazioni genetiche?'.